Ученые создали «грузовик», который доставляет генетические пакеты в мозг
Созданные учеными системы доставки генетического материала представляют собой важный шаг в направлении генной терапии для мозга, способной безопасно и точно корректировать неправильную мозговую активность. Результаты исследования были опубликованы в журнале Neuron.
Новый метод открывает для исследователей возможности создания систем доставки генов для различных видов животных, используемых в научных исследованиях. На сегодняшний день процесс создания генетически модифицированных или трансгенных животных является длительным и затратным. В качестве примера можно отметить использование флуоресцентных белков для визуализации тонких структур клеток мозга, а также активацию или подавление нейронных цепей, отвечающих за поведение и когнитивные функции.
«Представьте эту новую платформу как грузовик, который доставляет специализированные генетические пакеты в конкретные области головного и спинного мозга, — объясняет нейробиолог Джон Нгай, директор программы The BRAIN Initiative. — С помощью таких систем доставки мы теперь можем достигать определенных клеток головного и спинного мозга и управлять ими — этот уровень доступа ранее был недоступен в таких масштабах».
Новые инструменты на основе рекомбинантного аденоассоциированного вируса (rAAV) для доставки ДНК в целевые клетки могут быть широко использованы в различных экспериментальных системах, включая небольшие образцы тканей, получаемые во время нейрохирургии. Эти системы уже успешно протестированы на живых организмах, что открывает путь для их более широкого применения.
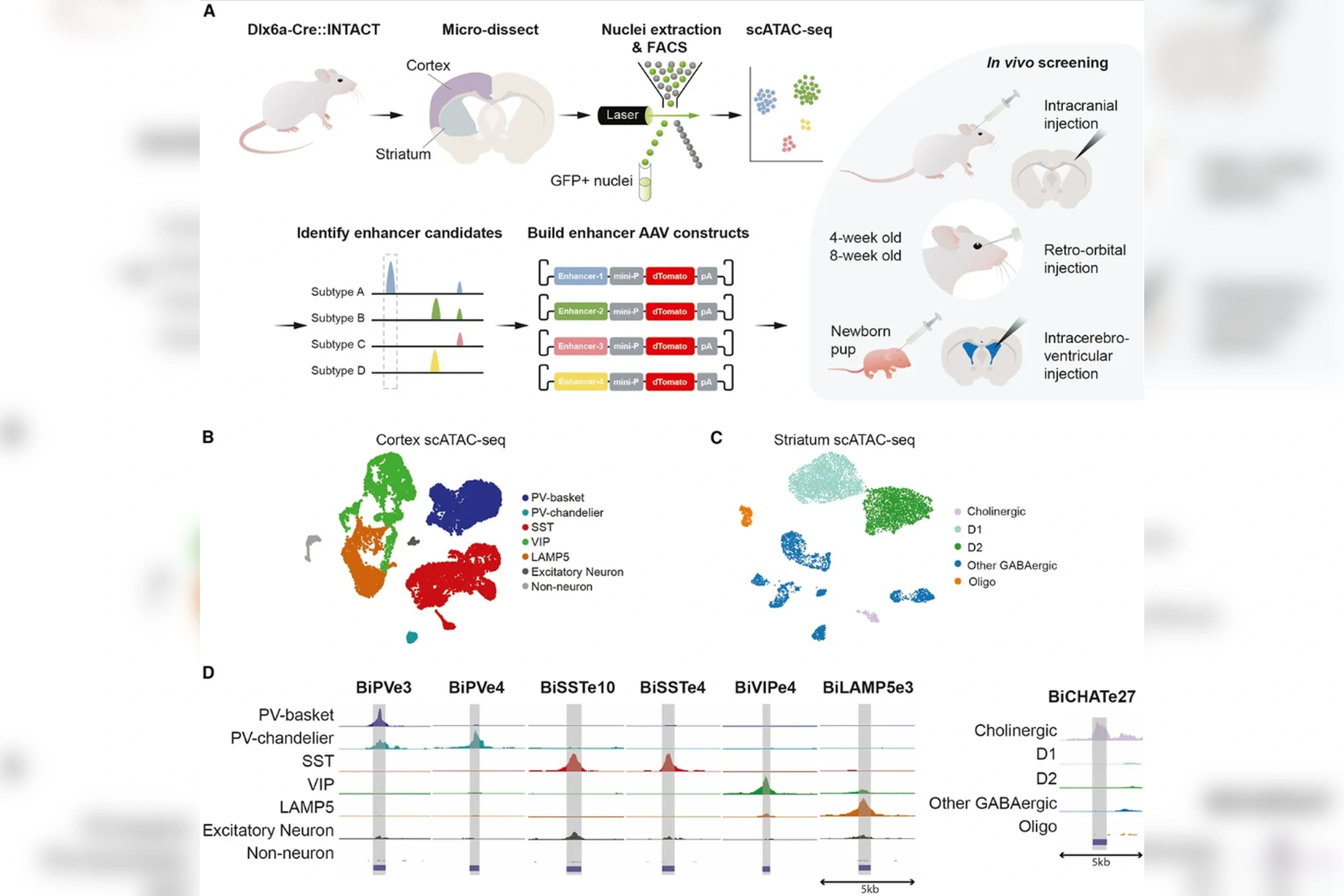
Набор инструментов включает множество систем доставки, которые нацелены на ключевые типы клеток мозга, среди которых возбуждающие нейроны, тормозные интернейроны, клетки кровеносных сосудов и труднодоступные нейроны спинного мозга. Эти нейроны, отвечающие за управление движением, подвергаются повреждениям при таких серьезных неврологических заболеваниях, как боковой амиотрофический склероз (БАС) и спинальная мышечная атрофия.
Ученые разработали когнитивные программы на основе ИИ, которые способны выявлять генетические усилители (энхансеры), активирующие гены в определенных типах клеток мозга. Стоит отметить, что этот инструмент предоставляет доступ к нейронам префронтальной коры — области, критически важной для принятия решений и уникальных характеристик человека.
С помощью инструментов из этой коллекции ученые получат возможность более детально исследовать отдельные клетки и коммуникационные пути, которые поражаются при ряде неврологических заболеваний. К числу этих заболеваний относятся судорожные расстройства, боковой амиотрофический склероз, болезнь Паркинсона, болезнь Альцгеймера и болезнь Хантингтона, а также различные нейропсихиатрические расстройства.
Методы лечения, основанные на рекомбинантной аденоассоциированной вирусной векторной терапии (rAAV), уже получили одобрение для лечения некоторых заболеваний, таких как спинальная мышечная атрофия.
В 2016 году был одобрен препарат генотерапии под названием Zolgensma, который изменил жизнь младенцев и маленьких детей, ранее сталкивавшихся с тяжелой инвалидностью или риском ранней смерти. Однако стоимость Zolgensma является весьма высокой: одна инъекция обходится в $2,1 млн.
Новые подходы к генной терапии могут значительно снизить ее стоимость. Эти методы действуют схожим с Zolgensma образом, а в будущем они могут даже превзойти его по эффективности. Основываясь на той же платформе (рекомбинантные аденоассоциированные вирусные векторы), эти инновации применяют технологии искусственного интеллекта. Что позволяет достичь высокой клеточной специфичности и, в свою очередь, открывает возможности для более точной и персонализированной терапии различных заболеваний головного и спинного мозга, включая спинальную мышечную атрофию.
Новая коллекция ресурсов для доставки генов служит основой для разработки целевых методов лечения, которые направлены исключительно на пораженные клетки в головном и спинном мозге, а также на сосудистую систему головного мозга.








